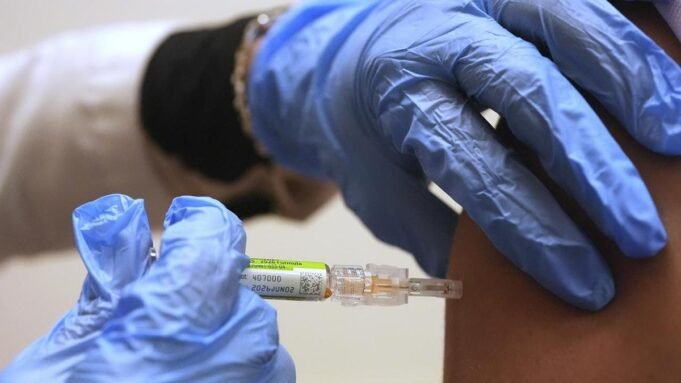
Amerykańska Agencja ds. Żywności i Leków odmawia rozpatrzenia wniosku firmy Moderna dotyczącego nowej szczepionki przeciw grypie wykonanej w technologii mRNA, która zdobyła Nagrodę Nobla.
Ta wiadomość jest najnowszym sygnałem wzmożonej kontroli FDA nad szczepionkami pod rządami Sekretarza Zdrowia Roberta F. Kennedy’ego Jr., zwłaszcza tych wykorzystujących technologię mRNA, które krytykował zarówno przed objęciem stanowiska najwyższego urzędnika ds. zdrowia w kraju, jak i po nim.
Firma Moderna otrzymała od FDA pismo „odmowa złożenia wniosku”, w którym sprzeciwiła się temu, jak przeprowadziła badanie kliniczne na 40 000 osobach, porównujące jej nową szczepionkę z jedną ze standardowych obecnie stosowanych szczepionek przeciw grypie.
Poznaj aktualności dzięki aplikacji 7NEWS: Pobierz już dziś
W badaniu tym stwierdzono, że nowa szczepionka jest nieco skuteczniejsza u osób dorosłych w wieku 50 lat i starszych niż standardowa szczepionka.
W piśmie dyrektora ds. szczepionek FDA, dr Vinaya Prasada, stwierdzono, że agencja nie uważa wniosku za zawierającego „odpowiednie i dobrze kontrolowane badanie”, ponieważ nie porównała nowego szczepionki z „najlepszym dostępnym standardem opieki w Stanach Zjednoczonych w czasie badania”.
W piśmie Prasad wskazano na pewne rady, których urzędnicy FDA udzielili firmie Moderna w 2024 r. pod administracją Bidena, których Moderna nie zastosowała.
Według firmy Moderna z opinii tych wynika, że dopuszczalne jest stosowanie wybranej przez firmę szczepionki przeciw grypie w standardowej dawce, ale w przypadku wszystkich osób w wieku 65 lat i starszych objętych badaniem preferowana byłaby inna marka, specjalnie zalecana seniorom.
Mimo to, Moderna stwierdziła, że FDA zgodziła się na kontynuowanie badania zgodnie z pierwotnym planem.
Firma podała, że udostępniła FDA dodatkowe dane z oddzielnego badania porównującego nową szczepionkę z licencjonowanym zastrzykiem o dużej dawce stosowanym u seniorów.
FDA „nie stwierdziła żadnych obaw dotyczących bezpieczeństwa lub skuteczności naszego produktu” i „nie realizuje naszego wspólnego celu, jakim jest wzmocnienie wiodącej pozycji Ameryki w opracowywaniu innowacyjnych leków”, stwierdziła we wtorkowym oświadczeniu dyrektor generalny Moderny Stephane Bancel.
Rzadko zdarza się, aby FDA odmawiała złożenia wniosku, szczególnie w przypadku nowej szczepionki, co wymaga od firm i pracowników FDA angażowania się w wielomiesięczne lub lata dyskusje.
Moderna zwróciła się o pilne spotkanie z FDA i zauważyła, że złożyła wniosek o zatwierdzenie szczepionki w Europie, Kanadzie i Australii.
W zeszłym roku urzędnicy FDA pracujący pod przewodnictwem Kennedy’ego wycofali zalecenia dotyczące szczepionek na Covid-19, dodali dodatkowe ostrzeżenia do dwóch wiodących szczepionek na Covid – wykonanych w technologii mRNA – i usunęli krytyków podejścia administracji z panelu doradczego FDA.
W zeszłym roku Kennedy ogłosił, że jego wydział anuluje kontrakty i finansowanie o wartości ponad 500 milionów dolarów (707 milionów dolarów) na rozwój szczepionek wykorzystujących mRNA.